cho 200g dung dịch NAOH 4% vào 200g dung dịch H2SO4 9,8% . tính nồng độ phần trăm các chất trong dung dịch sau phản ứng

Những câu hỏi liên quan
B1: Cho 300g dung dịch H2SO4 19,6 % tác dụng với 200g dug dịch NaOH 20%
a) Viết PTHH
b) Tính nồng độ phần trăm của các chất trong dung dịch sau phản ứng
a. PTHH: H2SO4 + 2NaOH ---> Na2SO4 + 2H2O
b. Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{m_{H_2SO_4}}{300}.100\%=19,6\%\)
=> \(m_{H_2SO_4}=58,8\left(g\right)\)
=> \(n_{H_2SO_4}=\dfrac{58,8}{98}=0,6\left(mol\right)\)
Ta lại có: \(C_{\%_{NaOH}}=\dfrac{m_{NaOH}}{200}.100\%=20\%\)
=> mNaOH = 40(g)
=> \(n_{NaOH}=\dfrac{40}{40}=1\left(mol\right)\)
Ta thấy: \(\dfrac{0,6}{1}>\dfrac{1}{2}\)
Vậy H2SO4 dư.
=> \(m_{dd_{Na_2SO_4}}=300+40=340\left(g\right)\)
Theo PT: \(n_{Na_2SO_4}=\dfrac{1}{2}.n_{NaOH}=\dfrac{1}{2}.1=0,5\left(mol\right)\)
=> \(m_{Na_2SO_4}=0,5.142=71\left(g\right)\)
=> \(C_{\%_{Na_2SO_4}}=\dfrac{71}{340}.100\%=20,88\%\)
Đúng 0
Bình luận (0)
Trộn 200g dung dịch nạo 4% với 200g dung dịch HCl 7,3%. Tính nồng độ phần trăm các chất tan có trong dung dịch sau phản ứng
\(n_{NaOH}=\dfrac{200.4\%}{40}=0,2\left(mol\right)\\ n_{HCl}=\dfrac{200.7,3\%}{36,5}=0,4\left(mol\right)\\ NaOH+HCl\rightarrow NaCl+H_2O\\ m_{ddsau}=200+200=400\left(g\right)\\ Vì:\dfrac{0,2}{1}< \dfrac{0,4}{1}\Rightarrow HCldư\\ n_{HCl\left(p.ứ\right)}=n_{NaCl}=n_{NaOH}=0,2\left(mol\right)\\ n_{HCl\left(dư\right)}=0,4-0,2=0,2\left(mol\right)\\ C\%_{ddHCl\left(dư\right)}=\dfrac{0,2.36,5}{400}.100=1.825\%\\ C\%_{ddNaCl}=\dfrac{0,2.58,5}{400}.100=2,925\%\)
Đúng 2
Bình luận (0)
NaCl+HCl→NaCl+H2O
nHCl=300.7,3%/36,5=0,6>nNaOH=200.4%/40=0,2→HCl dư
nHCl pư=nNaCl=nNaOH=0,2(mol)
nHCl dư=0,6−0,2=0,4(mol)
mdd sau pư=300+200=500(gam)
C%NaCl=0,2.58,5500.100%=2,34%
C%HCl=0,4.36,5500.100%=2,92%
Đúng 0
Bình luận (1)
1. Cho 6,5g Zn vào 200g dung dịch H2SO4 loãng có nồng độ 4,9%
a. Hỏi có chất nào dư sau phản ứng? Dư bao nhiêu mol?
b. Hỏi thu được bao nhiêu mol muối tạo thành?
c. Tính nồng độ phần trăm của các chất tạo trong dung dịch sau phản ứng. Coi như thể tích dung dịch không đổi
PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
a) Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\n_{H_2SO_4}=\dfrac{200\cdot4,9\%}{98}=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Cả 2 chất p/ứ hết
b+c) Theo PTHH: \(n_{ZnSO_4}=n_{H_2}=n_{Zn}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{ZnSO_4}=0,1\cdot161=16,1\left(g\right)\\m_{H_2}=0,1\cdot2=0,2\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{Zn}+m_{ddH_2SO_4}-m_{H_2}=206,3\left(g\right)\)
\(\Rightarrow C\%_{ZnSO_4}=\dfrac{16,1}{206,3}\cdot100\%\approx7,8\%\)
Đúng 1
Bình luận (0)
a,tính khối lượng NaOH có trong 200ml dung dịch NaOh 1M b,tính số mol H2SO4 có trong 100ml dung dịch H2SO4 2M c,hoà tan 6g NaCl vào nước thu được 200g dung dịch tính nồng độ phần trăm của dung dịch d,tính khối lượng NaCl có trong 200g dung dịch NaCl 8%
a, \(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
\(m_{NaOH}=0,2.40=8\left(g\right)\)
b, \(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
\(c,C\%=\dfrac{6}{200}.100\%=3\%\)
\(m_{NaCl}=\dfrac{200.8}{100}=16\left(g\right)\)
Đúng 1
Bình luận (0)
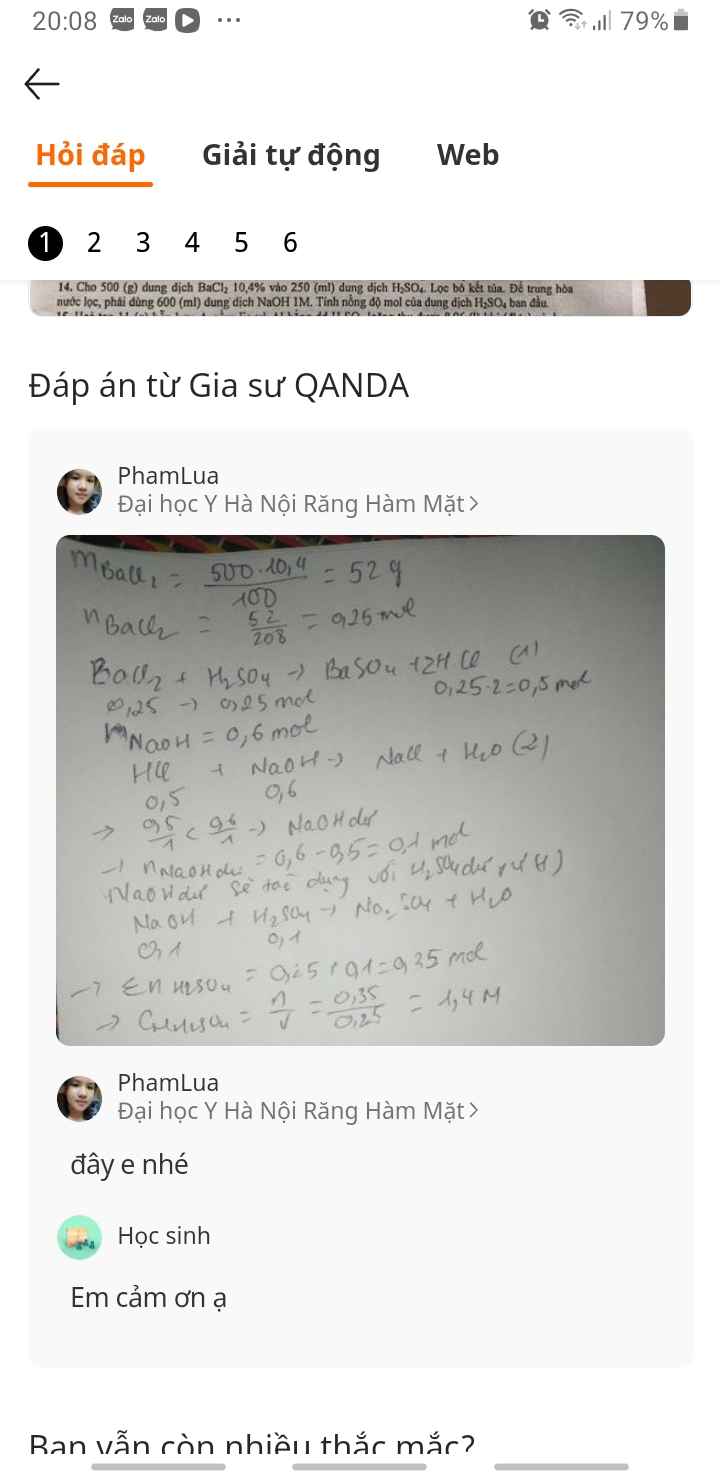
Cho 200g dung dịch Ba(OH)2 10o/o vào 200g dung dịch H2SO4. lọc bỏ kết tủa, trung hòa nước lọc cần dùng 250ml NaOH 25 o/o d = 1,28. Tính nồng độ o/o của dung dịch H2SO4 ban đầu và nồng độ o/o của dung dịch sau phản ứng?
Em ko có tiền nên mong a , cj tham khảo(đây là 500 g dung dịch nên mong a, cj sửa 1 chút ạ)
Đúng 1
Bình luận (1)
Cho 6g Mgo tác dụng với 200g dung dịch H2so4 19,6% tính nồng độ % các chất trong dung dịch sau phản ứng
nMgO=0,15(mol); nH2SO4=0,4(mol)
PTHH: MgO + H2SO4 -> MgSO4 + H2O
0,15________0,15__________0,15(mol)
Ta có: 0,15/1 < 0,4/1
=> H2SO4 dư, MgO hết, tính theo nMgO
-> nH2SO4(dư)=0,4-0,15=0,25(mol) => mH2SO4(dư)=24,5(g)
nMgSO4=nMg=0,15(mol) => mMgSO4=120.0,15=18(g)
mddsau=6+200=206(g)
=>C%ddH2SO4(dư)=(24,5/206).100=11,893%
C%ddMgSO4=(18/206).100=8,738%
Đúng 5
Bình luận (3)
PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\\n_{H_2SO_4}=\dfrac{200\cdot19,6\%}{98}=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit dư
\(\Rightarrow\left\{{}\begin{matrix}n_{MgSO_4}=n_{H_2}=0,25\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{MgSO_4}=0,25\cdot120=30\left(g\right)\\m_{H_2}=0,25\cdot2=0,5\left(g\right)\\m_{H_2SO_4\left(dư\right)}=0,15\cdot98=14,7\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{Mg}+m_{ddH_2SO_4}-m_{H_2}=205,5\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgSO_4}=\dfrac{30}{205,5}\cdot100\%\approx14,6\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{14,7}{205,5}\cdot100\%\approx7,2\%\end{matrix}\right.\)
Đúng 0
Bình luận (1)
Số mol của magie
nMg = \(\dfrac{m_{Mg}}{M_{Mg}}=\dfrac{6}{24}=0,25\left(mol\right)\)
Khối lượng của axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{19,6.200}{100}=39,2\left(g\right)\)
Số mol của axit sunfuric
nH2SO4 = \(\dfrac{m_{H2SO4}}{M_{H2SO4}}=\dfrac{39,2}{98}=0,4\left(mol\right)\)
Pt : MgO + H2SO4 → MgSO4 + H2O\(|\)
1 1 1 1
0,25 0,4 0,25
Lập tỉ số so sánh : \(\dfrac{0,25}{1}< \dfrac{0,4}{1}\)
⇒ MgO phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol MgO
Số mol của magie sunfat
nMgSO4 = \(\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
Khối lượng của magie sunfat
mMgSO4 = nMgSO4 . MMgSO4
= 0,25 . 120
= 30 (g)
Số mol dư của dung dịch axit sunfuric
ndư = nban đầu - nmol
= 0,4 - (0,25.1)
= 0,15 (mol)
Khối lượng dư của dung dịch axit sunfuric
mdư = ndư . MH2SO4
= 0,15 . 98
= 14,7 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mMgO + mH2SO4
= 6 + 200
= 206 (g)
Nồng độ phần trăm của magie sunfat
C0/0MgSO4 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{30.100}{206}=14,56\)0/0
Nồng độ phần trăm của dung dịch axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{14,7.100}{206}=7,14\)0/0
Chúc bạn học tốt
Đúng 3
Bình luận (2)
Xem thêm câu trả lời
: Trung hòa 200g dung dịch NaOH nồng độ 10% bằng dung dịch axit sunfuric nồng độ 20%.
Viết PTPU và tính khối lượng dung dịch axit sunfuric.
Tính nồng độ phần trăm dung dịch muối sau phản ứng
\(m_{ct}=\dfrac{10.200}{100}=20\left(g\right)\)
\(n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right)\)
a) Pt : \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O|\)
2 1 1 2
0,5 0,25 0,25
\(n_{H2SO4}=\dfrac{0,5.1}{2}=0,25\left(mol\right)\)
\(m_{H2SO4}=0,25.98=24,5\left(g\right)\)
\(m_{ddH2SO4}=\dfrac{24,5.100}{20}=122,5\left(g\right)\)
b) \(n_{Na2SO4}=\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
⇒ \(m_{Na2SO4}=0,25.142=35,5\left(g\right)\)
\(m_{ddspu}=200+122,5=322,5\left(g\right)\)
\(C_{Na2SO4}=\dfrac{35,5.100}{322,5}=11\)0/0
Chúc bạn học tốt
Đúng 4
Bình luận (1)
: Trung hòa 200g dung dịch NaOH nồng độ 10% bằng dung dịch axit sunfuric nồng độ 20%.
A Viết PTPU và tính khối lượng dung dịch axit sunfuric.
B Tính nồng độ phần trăm dung dịch muối sau phản ứng
cho 4 gam đồng (II) õit tác dụng với 200g dung dịch HCl có nồng độ 3,65%
a) biết phương trình hoá học
b) tính nồng độ phần trăm của các chất có trong dung dịch sau khi phản ứng kết thúc
\(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
\(m_{ct}=\dfrac{3,65.200}{100}=7,3\left(g\right)\)
\(n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\)
a) Pt : \(CuO+2HCl\rightarrow CuCl_2+H_2O|\)
1 2 1 1
0,05 0,2 0,05
b) Lập tỉ số so sánh : \(\dfrac{0,05}{1}< \dfrac{0,2}{2}\)
⇒ CuO phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của CuO
\(n_{CuCl2}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
⇒ \(m_{CuCl2}=0,05.135=6,75\left(g\right)\)
\(n_{HCl\left(dư\right)}=0,2-\left(0,05.2\right)=0,1\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)
\(m_{ddspu}=4+200=204\left(g\right)\)
\(C_{CuCl2}=\dfrac{6,75.100}{204}=3,31\)0/0
\(C_{HCl\left(dư\right)}=\dfrac{3,65.100}{204}=1,8\)0/0
Chúc bạn học tốt
Đúng 2
Bình luận (0)

























